| Abschnitt | Beschreibung |
|---|---|
| Titel | Eine prospektive randomisierte Phase-I/II-Studie zur Behandlung von Patienten mit rezidivierter oder refraktärer chronisch lymphatischer Leukämie (CLL) oder Kleinzelligem lymphozytischem Lymphom (SLL) mit Venetoclax (26 Zyklen) und 6 oder 12 Zyklen Epcoritamab (AETHER Studie) |
| Studienkennung/ Identifier | Protokoll Code: HOVON165 CLL EUCT: 2022-500305-40 NCT05791409 |
| Teilnehmende Länder | Niederlande, Belgien, Dänemark, Deutschland, Australien |
Status | RekrutierendPhase I – nur in NL und DK (beendet) Phase II – aktiv (seit Februar 2025) |
| Kontakt | cll-ho165@uk-koeln.de |
| Design | Prospektive, 2-armige, offene, multizentrische, randomisierte Phase I/II-Studie |
| Primärer Endpunkt | Bewertung der Wirksamkeit der Behandlung mit Venetoclax (26 Zyklen) in Kombination mit 6 Zyklen oder 12 Zyklen Epcoritamab bei Patienten mit rezidivierter oder refraktärer CLL im Hinblick auf eine nicht messbare/minimale Resterkrankung <10-4 (undetectable residual disease, uMRD4) im Knochenmark (BM) |
| Sekundäre Endpunkte |
|
| Studienpopulation | Patienten mit einer rezidivierten oder refraktären chronisch lymphatischen Leukämie (CLL) oder kleinzelligem lymphozytischen Lymphom (SLL) nach mindestens einer vorangegangenen Behandlungslinie (diese kann auch eine Therapie mit einem Bruton-Tyrosinkinase-Inhibitor und/oder Venetoclax umfassen). Im Falle einer vorherigen Venetoclax-Behandlung kann die Aufnahme in diese Studie erst mindestens 24 Monate nach Abschluss der Venetoclax-Behandlung erfolgen. |
| Therapie / Therapiearme | Arm A (Venetoclax 26 Zyklen und Epcoritamab 6 Zyklen) Aufdosierung Venetoclax (5 Wochen) Tag 1-7: Venetoclax 20mg (2 Tabl. à 10 mg) Tag 8-14: Venetoclax 50mg (1 Tabl. à 50 mg) Tag 15-21: Venetoclax 100 mg (1 Tabl. à 100 mg) Tag 22-28: Venetoclax 200 mg (2 Tabl. à 100 mg) Tag 39-35: Venetoclax 400 mg (4 Tabl. à 100 mg) Zyklus 1-26 – Venetoclax Tag 1-28: Venetoclax 400 mg (4 Tabl. à 100 mg) + Zyklus 1-6 – Epcoritamab Zyklus 1: Tag 1: Epcoritamab (Injektion 0.16 mg) Tag 8: Epcoritamab (Injektion 0.8 mg) Tag 15: Epcoritamab (Injektion 3 mg) Tag 22: Epcoritamab (Injektion 48 mg) Zyklus 2+3: Tag 1, 8, 15, 22: Epcoritamab (Injektion 48 mg) Zyklus 4-6: Tag 1, 15: Epcoritamab (Injektion 48 mg) Arm B (Venetoclax 26 Zyklen und Epcoritamab 12 Zyklen) Aufdosierung Venetoclax (5 Wochen) Tag 1-7: Venetoclax 20mg (2 Tabl. à 10 mg) Tag 8-14: Venetoclax 50mg (1 Tabl. à 50 mg) Tag 15-21: Venetoclax 100 mg (1 Tabl. à 100 mg) Tag 22-28: Venetoclax 200 mg (2 Tabl. à 100 mg) Tag 39-35: Venetoclax 400 mg (4 Tabl. à 100 mg) Zyklus 1-26 – Venetoclax Tag 1-28: Venetoclax 400 mg (4 Tabl. à 100 mg) + Zyklus 1-12 – Epcoritamab Zyklus 1: Tag 1: Epcoritamab (Injektion 0.16 mg) Tag 8: Epcoritamab (Injektion 0.8 mg) Tag 15: Epcoritamab (Injektion 3 mg) Tag 22: Epcoritamab (Injektion 48 mg) Zyklus 2+3: Tag 1, 8, 15, 22: Epcoritamab (Injektion 48 mg) Zyklus 4-9: Tag 1, 15: Epcoritamab (Injektion 48 mg) Zyklus 10-12: Tag 1: Epcoritamab (Injektion 48 mg) 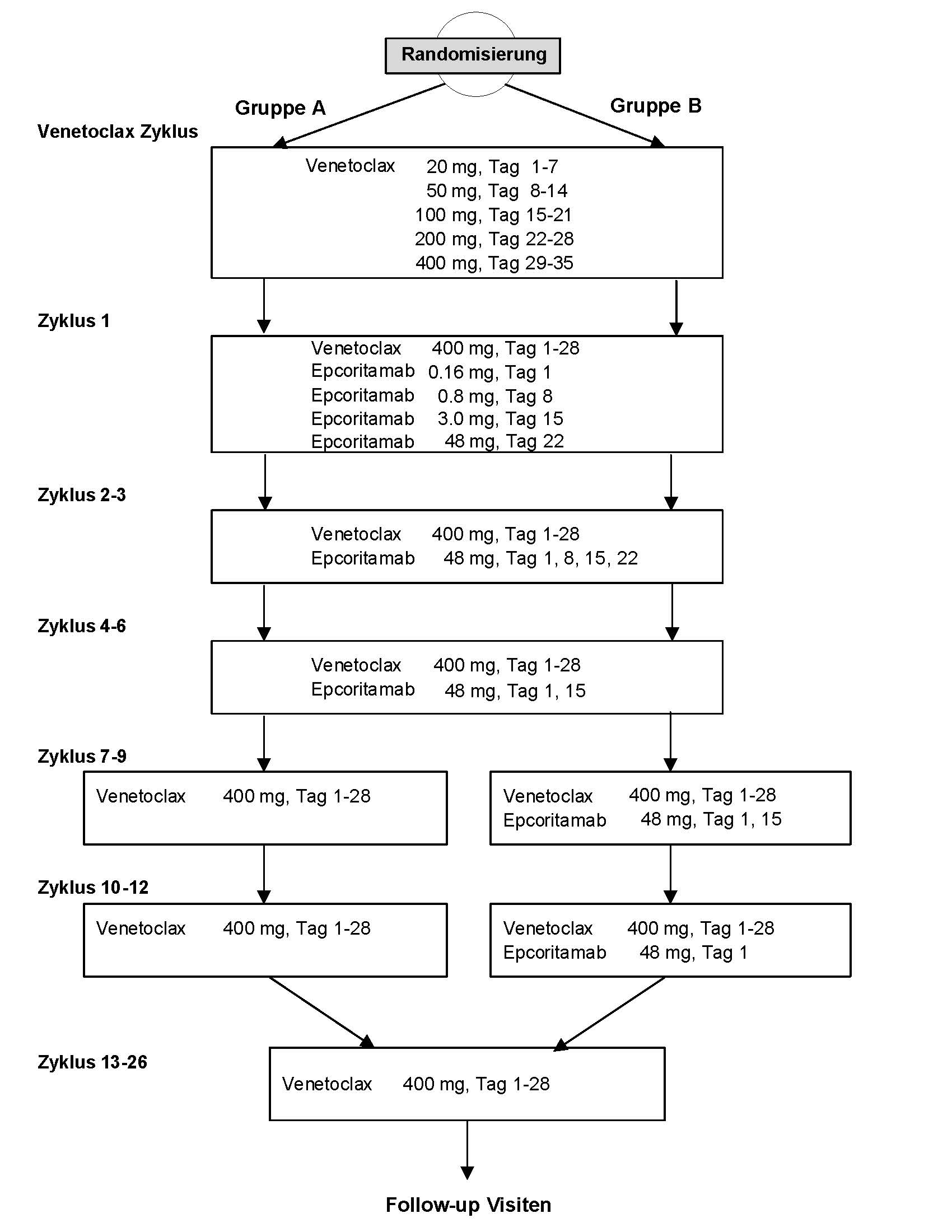 |
| Erforderliche Patientenzahl | 100 |
| Aktuell eingeschlossene Patienten | 51 |
| Zeitplan | Rekrutierungsstart: Q1/2025 |
| Sponsor | HOVON |
| Studienleitung | Dr. med. Arnon P. Kater, Amsterdam UMC, Department of Hematology, Cancer Center Amsterdam |
| Coordinating Investigators (DE) | Prof. Dr. med. Barbara Eichhorst und Dr. med. Kirsten Fischer, Klinik I für Innere Medizin, Uniklinik Köln |
| Download | n.n. |
