| Abschnitt | Beschreibung |
|---|---|
| Titel | Eine Phase I/II Studie mit NCT-CART20 bei Patienten mit CD20-positiven B-Zell-Lymphomen |
| Studienkennung/Identifer | Protokoll-Code: NCT-CART20 EUCT: tbd |
| Teilnehmende Länder | Deutschland |
Status | Geplant |
| Kontakt | nct-cart20@uk-koeln.de |
| Design | Prospektive, offene, multizentrische Phase-I/II-Studie |
| Primärer Endpunkt | • Phase I Kohorte a+b zur Bewertung der empfohlenen Phase-II-Dosis (RP2D) und der Durchführbarkeit bei Patienten mit klonaler Lymphozytose • Phase II: die Wirksamkeit von NCT-CART20 in vordefinierten Untergruppen mit hohem ungedecktem medizinischem Bedarf zu bewerten |
| Sekundärer Endpunkt | • Bewertung des Sicherheitsprofils und der Durchführbarkeit von NCT-CART20 • Zur Bewertung der Wirksamkeit anhand von Überlebensparametern • Auswertung der Pharmakokinetik von NCT-CART20 • Auswertung der Lebensqualitätsergebnisse |
| Studienpopulation | Patienten mit rezidiviertem/refraktärem Lymphom bei denen CD19-gerichtete CAR-Therapien versagt haben oder die nicht für diese Therapien qualifizieren. Außerdem sollen Patienten mit seltenen, aggressiven Lymphom-Entitäten eingeschlossen werden, für die es derzeit keine zugelassene CAR-T-Zell-Therapie gibt, wie z. B. die Richter-Transformation (einer CLL in ein diffuses großzelliges B-Zelllymphom; DLBCL-RT) oder das rezidivierte noduläre lymphozytenprädominante Hodgkin-Lymphom (NLPHL) nach Versagen von mindestens zwei Vortherapien. |
| Therapie / Therapiearme | 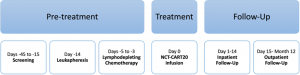 |
| Erforderliche Patientenzahl | Phase I cohort a: mind. 6 – max. 12 Patienten Phase I cohort b: mind. 3 – max. 6 Patienten Phase II: 31 Patienten (davon mind. 5 pro Kohorte) |
| Zeitplan | Rekrutierungsstart: Q1/2027 |
| Sponsor | Universität zu Köln |
| Studienleitung | PD Dr. Nadine Kutsch |
| Investigators (DE) | PD Dr. Nadine Kutsch, Uniklinik Köln Prof. Bastian von Tresckow, Uniklinik Essen Prof. Fabian Müller, Uniklinik Erlangen Prof. Ulrich Keller, Charité Universitätsmedizin Berlin Prof. Max Topp, Uniklinik Würzburg |
